Inicio: 5 de Mayo 2025


CURSO DE PREPARACIÓN PARA LA CERTIFICACIÓN DE AUDITOR DE DISPOSITIVOS MÉDICOS
DESCRIPCIÓN:
¿POR QUÉ CONVERTIRSE EN UN AUDITOR DE DISPOSITIVOS MÉDICOS CERTIFICADO?
Como Auditor Certificado de Dispositivos Médicos (CMDA), será un profesional que comprende los principios de los estándares, regulaciones, directivas y orientación para auditar un sistema de dispositivos médicos mientras utiliza diversas herramientas y técnicas para examinar, cuestionar, evaluar e informar sobre las adecuaciones y deficiencias de ese sistema. Un CMDA analiza todos los elementos del sistema e informa sobre el grado en que se adhiere a los criterios de gestión y control de la seguridad de los procesos.
¿CUÁLES SON LAS COMPETENCIAS BÁSICAS DE UN CMDA?
Comprender los diferentes tipos de auditorías, las funciones y responsabilidades de la auditoría, y los problemas éticos, legales y profesionales asociados con las auditorías.
Aplicar y comprender una amplia variedad de requisitos del sistema de gestión de calidad de dispositivos médicos, incluidas las leyes y regulaciones regulatorias de EE. UU. y extranjeras (por ejemplo, Código de Regulaciones Federales, 21 CFR 820) y estándares internacionales de calidad (por ejemplo, ISO 9001, ISO 13485).
Comprenda las herramientas de calidad, como los diagramas de Pareto, los diagramas de causa y efecto, los diagramas de flujo, los gráficos de control estadístico de procesos (SPC), las hojas de comprobación, los diagramas de dispersión, los histogramas y el plan-hacer-verificar-actuar (PDCA).
Identificar y aplicar normas relacionadas con la gestión de riesgos, la detección de peligros y la esterilización para productos procesados asépticamente y esterilizados terminalmente.
Evalúe los programas de gestión de riesgos y los requisitos para el manejo de quejas, la vigilancia, los informes de dispositivos médicos (MDR) y los procesos de seguimiento y retiro de productos. Revisar los procedimientos de validación para las pruebas de laboratorio y utilizar los métodos adecuados para analizar, detectar y controlar las no conformidades.
Identificar y describir los términos de biocompatibilidad y la justificación de la selección de pruebas de acuerdo con las normas y directrices aplicables. Evalúe los controles ambientales y determine si los servicios públicos requieren calificación, validación o mantenimiento.
Reconocer los elementos del ciclo de vida del desarrollo de software para productos, procesos y sistemas de calidad.
I. Auditing Fundamentals
A. Tipos de Auditoría:
- Auditorías por método
- Auditorías por propósito.
B. Funciones y responsabilidades de la auditoría.
C. Ético, legalidad y problemas profesionales
- Conducta y responsabilidades profesionales.
- Consecuencias legales y responsabilidad.
II. Conocimiento técnico biomédico
A. Preparación y planificación de auditorías:
- Elementos del proceso de planificación de auditoría.
- Selección del auditor.
- Documentación relacionada con la auditoría.
- Herramientas de auditoría.
- Estrategias de auditoría.
- Logistics.
B. Rendimiento de auditoría
- Reunión de apertura.
- Recogida y análisis de datos.
- Técnicas de comunicación.
- Organización y análisis de evidencia objetiva.
- Gestión de auditoría en el sitio.
- Salir de la reunión.
C. Informes de auditoría
- Elementos básicos.
- Informes de auditoría efectivos.
- Retención de registros.
D. Seguimiento de auditoría y cierre
- Elementos de las acciones correctivas y preventivas.
- Revisión del plan de acción correctiva.
- Realización de seguimiento de auditoría.
- Cierre de auditoría.
E. Referencias de procedimiento de auditoría
- Directrices internacionales para auditar sistemas de calidad.
- Quality System InspectionTechnique (QSIT) y FDA CPG 7382.845.
III. Requisitos del sistema de gestión de calidad biomédica
A. Leyes regulatorias y requisitos
- FDA – Código de Regulaciones Federales (CFR) Título 21.
- Requisitos de EE. UU. (Ley FD & C, 201, 301-304, 501-502, 510, 513, 518, 704).
- Directiva europea: Directiva sobre dispositivos médicos 93/42 / EEC (MDD) 14 de junio de 1993 (Artículo 1) modificada por la Directiva 2007/47 / CE..
- Health Canada.
- Japón.
- Otras agencias internacionales.
B. Guía de la FDA para la fabricación de productos (IVD)
C. Estándares internacionales para sistemas de calidad
- ISO 9001, ISO 13485, ISO 17025.
- GHTF.SG3.N99-10.
D. Requisitos de Regulación del Sistema de Calidad (QSR) (21 CFR 820 – Partes como se muestra)
- Responsabilidad de gestión (Partes 20, 22, 25).
- Sistema de control de diseño (Parte 30).
- Documento (Parte 40) y control de registro (Partes 180-186).
- Controles de compra y actividades de aceptación (Partes 50, 80, 86).
- Identificación y trazabilidad (Partes 60, 65).
- Controles de producción y proceso (Partes 70, 72, 75).
- Producto no conforme (Parte 90).
- Sistema de acción correctiva y preventiva (CAPA) (Parte 100).
- Manejo, almacenamiento, distribución e instalación del producto (Partes 140-170).
- Servicio (Parte 200).
- Técnicas estadísticas (Parte 250) .
E. Vigilancia posterior al mercado (Orientación bajo la Sección 522 de la Ley FD & C)
IV. Conocimiento biomédico técnico
A. Gestión de riesgos
- ISO 14971.
- IEC 62366.
B. Esterilización
- Definiciones.
- Métodos y controles de proceso.
C. Biocompatibilidad
D. Ambientes controlados y sistemas de utilidad
- Ambientes controlados.
- Sistemas de utilidad.
E. Desarrollo y mantenimiento de software para productos
F. Pruebas de laboratorio y análisis de fallas
G. Fuentes para estándares nuevos y en desarrollo
H. Directivas y estándares comunes de dispositivos médicos
- IEC 60601-1 and IEC 80001.
- Directiva de Restricción de Sustancias Peligrosas (RoHS).
- Registro, Evaluación, Autorización y Restricción de Productos Químicos (REACH).
- Residuos de aparatos eléctricos y electrónicos (RAEE).
I. Packaging
J. Reprocesamiento / Reutilización y limpieza de dispositivos médicos
V. Herramientas y técnicas de calidad
A. Process Improvement Techniques
- ISO 14971.
- IEC 62366.
B. Técnicas de mejora de procesos
- Capacidad de procesamiento.
- Seis Sigma.
- Herramientas Lean.
- Análisis del Sistema de Medición (MSA).
- Costos de Calidad (COQ).
C. Tipos de datos y muestreo
- Análisis cualitativo y cuantitativo.
- Atributos y variables de datos.

¿CUÁL ES EL VALOR PARA SU EMPRESA TENER UN INTEGRANTE CON CONOCIMIENTOS DE CMDA?
Garantizar la conformidad con los estándares de la industria y el cumplimiento de las regulaciones y requisitos relacionados con los sistemas de calidad, quejas, MDR, clasificación de productos y más.
Comprender las herramientas de auditoría de la industria, como la Técnica de Inspección del Sistema de Calidad (QSIT) de la FDA y la auditoría basada en riesgos.
Mitigar los riesgos costosos utilizando métodos y procesos de esterilización adecuados.
Mejorar los procesos mediante la implementación de herramientas y técnicas de calidad.
¿CUÁL ES EL VALOR PARA TI ESTAR ENTRENADO Y CERTIFICADO COMO CMDA?
Un conjunto de habilidades mejorado lo califica para más puestos dentro de los entornos comerciales modernos.
Los CMDA con un título de trabajo de auditor ganan un promedio de $96,827 por año, en comparación con los auditores sin certificación, que ganan aproximadamente $73,975.
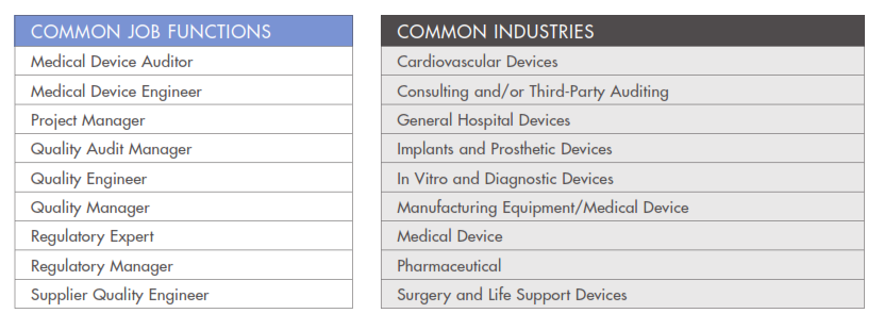
INFORMACIÓN DEL MERCADO DONDE LABORA UN CMDA
TENDENCIAS CLAVE DEL MERCADOS CLAVE DE UN CMDA
- Gestión de riesgos (ISO 14971)
- Toma de decisiones basada en el riesgo
- Cumplimiento de la norma FDA 21 CFR 820
- ISO 13485
IMPORTANTE
El participante debe tener conocimientos en el idioma inglés ya que el material y el examen son en este idioma.
Cómo establecer los requerimientos de la vestimenta en los cuartos limpios
En este blog le explicamos cómo usar la norma ISO 14644-5:2004 Cuartos limpios y entornos controlados asociados – Operaciones para establecer los requerimientos para la vestimenta en cuartos limpios.